Ige OA*
Bolaji BO
Kolawole IK
*Departments of Anaesthesia, Obafemi Awolowo University Teaching Hospital, Ile-Ife, Nigeria,
Department of Anaesthesia, University of Ilorin Teaching Hospital, Ilorin, Nigeria.
E-mail: femiigedoc@yahoo.com
Subvention de soutien: Aucune
Conflit d'intérêts: Aucun
RESUMÉ
FOND DE LÉTUDE : Le traitement de la douleur est traditionnellement fourni par des analgésiques morphiniques. Cependant, la réticence de certains personnels de santé à prescrire ou à administrer des opiacés par crainte des effets secondaires a entravé leur usage. Linfiltration danesthésique local dans la plaie est indiquée comme améliorant le traitement postopératoire de la douleur. BUTS ET OBJECTIFS : Déterminer lefficacité de linfiltration sous-aponévrotique et sous-cutanée combinée de bupivacaïne dans la provision dun effet dépargne morphinique suite à une chirurgie abdominale.
CONCEPTION DE LÉTUDE : Cest une étude de nature prospective, randomisée, en double aveugle, contrôlée par placebo. CADRE : Létude est menée au Centre Hospitalier Universitaire de lUniversité dIlorin, Ilorin, Nigéria.
PATIENTS ET MÉTHODES : Le groupe détude reçoit une infiltration sous-aponévrotique et sous-cutanée avec 40ml de 0,25% de bupivacaïne pendant que le groupe témoin reçoit 40ml de 0,9% de saline administrés par un chirurgien après la fermeture du péritoine. Lanalgésie postopératoire est fournie avec 1,0mg/kg de morphine intramusculaire à quatre heures dintervalle sur demande et lheure de la première demande analgésique est notée. Du paracétamol intraveineux est utilisé comme analgésie de secours.
La douleur postopératoire est évaluée en utilisant léchelle verbale simple (EVS) à 6, 12 et 24 heures postopératoires au repos et à la toux.
RÉSULTATS : Le temps moyen de la première demande analgésique est nettement prolongée (p<0,05) dans le groupe détude (174 ± 117,6 min) que dans le groupe témoin (102 ± 84min). Les patients dans le groupe témoin ont reçu plus de morphine, lequel nest pas statistiquement significatif (p>0,05). La demande dune analgésie de secours et limpression des patients sur lanalgésie ne sont pas significatives (Valeur p du test bilatéral exact de Fishers = 0,7164 et 0,4506 respectivement).
CONCLUSION : Linfiltration de bupivacaïne dans la plaie améliore les scores de douleur au repos dans les 6 premières heures et les scores de douleur à la toux dans les 24 premières heures postopératoires. Bien que la technique augmente les options disponibles pour le soulagement de la douleur postopératoire après une chirurgie abdominale basse, elle ne peut pas être utilisée seule dans ce type de chirurgie.
MOTS CLÉS : Opioïde, infiltration de bupivacaïne dans la plaie, chirurgie abdominale basse, analgésie postopératoire.
INTRODUCTION
Le traitement de la douleur fait partie importante des soins postopératoires des patients. Un soulagement effectif de la douleur postopératoire améliore le confort, entraîne une meilleure fonction respiratoire et un rapide rétablissement.1,2 Lanalgésie périopératoire est traditionnellement fournie par des analgésiques morphiniques tels que la péthidine ou la morphine. Cependant, les opiacés ont une variété deffets secondaires tels que la dépression ventilatoire, la sédation, la nausée et le vomissement, le prurit, la rétention urinaire, la constipation. Ceux-ci, en plus de la réticence de plusieurs professionnels de santé à prescrire ou à administrer des opiacés par crainte de la dépendance physique, associés à lapprovisionnement irrégulier des opiacés suite aux restrictions du gouvernement ont entraîné une prise en charge inadéquate de la douleur postopératoire au Nigéria. 1,2 Des chirurgies abdominales sont associées à deux types de douleur : une douleur sourde continue nauséabonde dorigine viscérale qui réagit bien aux opiacés, et une vive douleur somatique induite par la toux et le mouvement, qui réagit mal aux opiacés.3 Ainsi, quand un opiacé est utilisé seul pour traiter la douleur suite à une chirurgie abdominale, comme cest souvent le cas au Nigéria4, la composante somatique reste largement sous-traitée, entraînant une analgésie pauvre. Cette douleur peut entraîner une cicatrisation retardée5, une mauvaise fonction respiratoire6 et une douleur chronique.7 La contribution du traitement insuffisant de cette composante somatique a reçu peu dattention dans la littérature.
Linfiltration danesthésique locale dans la plaie est indiquée comme améliorant le traitement de la douleur après une large variété de procédures chirurgicales 8,9,10. Elle assure une bonne analgésie postopératoire dans les procédures chirurgicales superficielles telles que lherniorraphie, lamygdalectomie et lhémorroïdectomie. 11,12 Celles-ci sont des procédures avec peu ou pas de composante viscérale. Cependant, des enquêtes précédentes nont pas réussi à démontrer avec régularité un effet dépargne morphinique quand une anesthésie locale est infiltrée au site de lincision après une chirurgie abdominale. 13,14,15 Cette étude est destinée à déterminer lefficacité de linfiltration sous-aponévrotique et sous-cutanée combinée de bupivacaïne dans la provision dun effet dépargne morphinique suite à une chirurgie abdominale basse.
CADRE : Cette étude est menée au Centre Hospitalier Universitaire de lUniversité dIlorin, Ilorin, Nigéria. Cet hôpital est un centre de référence pour les patients de lEtat de Kwara et des Etats avoisinants de Kogi, de Niger, dEkiti et dOyo tous au Nigéria. ÉTENDUE DE LÉTUDE : Tous les patients prévus pour une myomectomie de confort et une hystérectomie abdominale totale dans la période détude sont inclus dans létude. TYPE DÉTUDE : Cest une étude de nature prospective, randomisée, en double aveugle et contrôlée par placebo.
PATIENTS ET MÉTHODES
La population de létude est composée de patients gynécologiques de statut ASA I ou II âgés dentre 16 et 65 ans qui sont prévus pour une hystérectomie ou une myomectomie de confort. Le problème : Traitement inadéquat de la douleur postopératoire.
Critère dexclusion : Des patients avec une maladie respiratoire antérieure, qui sont incapables de coopérer à cause de la barrière linguistique ou dun trouble psychiatrique et ceux qui sont sous traitement régulier avec des médicaments non-stéroïdiens anti-inflammatoires et des opiacés sont exclus de létude. Les patients qui ont refusé de participer à létude et ceux avec des antécédents dallergies à nimporte lequel des médicaments utilisés dans létude sont aussi exclus.
Chaque patient a été visité et évalué par le chercheur la nuit précédant lopération. Un consentement éclairé est obtenu après que les procédures aient été expliquées. On a aussi ordonné aux patients de demander de lanalgésie quand ils sentent de la douleur postopératoire. Un assistant chercheur a ensuite alloué par hasard les patients à lun des deux groupes (détude et de témoin) par tirage au sort.
Anesthésie
Une anesthésie générale standard est administrée. Les patients sont pré-oxygénés pour trois minutes et lanesthésie est provoquée avec 5mg/kg de thiopental sodique. 1mg/kg de suxaméthonium est administré par voie intraveineuse pour faciliter lintubation endotrachéale. La paralysie des muscles est maintenue avec 0,1mg/kg de pancuronium et des doses supplémentaires sont données comme il le faut. Les patients sont ventilés avec de loxygène de lair pour donner un FIO2 de 0,5% et ceci est complété avec 0,75% dhalotane ou disoflurane en utilisant le système respiratoire anesthésique de Bain. Lanalgésie intra-opératoire est fournie avec 1-3µg/kg de fentanyl donné par voie intraveineuse à linduction et maintenue avec des doses supplémentaires comme il le faut.
Après la fermeture du péritoine, les patients dans le groupe détude reçoivent une infiltration sous-cutanée et sous-aponévrotique avec 40ml de 0,25% de bupivacaïne à environ 1cm des berges de la plaie pendant que ceux dans le groupe de témoin reçoivent 40ml de 0,9% de saline administré de la même façon par le chirurgien qui est aveuglé à la solution utilisée. Les solutions pour linfiltration sont préparées et codées par une infirmière anesthésiste qui na joué aucun autre rôle dans létude. A la fin de lintervention chirurgicale, la paralysie des muscles est renversée avec 1,2mg datropine et 2,5mg de néostigmine.
Evaluation de la douleur
La douleur est évaluée dans la salle de rétablissement et la salle dobservation en utilisant léchelle verbale simple (EVS) pour la douleur (Appendice I). Dans la salle dobservation, la douleur est évaluée à 6, 12 et 24 heures à partir de la fin de lintervention chirurgicale. On a aussi demandé aux patients de décrire la douleur comme étant superficielle ou profonde. La douleur dynamique est évaluée en demandant aux patients de respirer profondément et de tousser. Lintensité de la douleur est notée. Vingt-quatre heures après lintervention chirurgicale, on a demandé aux patients leur degré de satisfaction concernant lanalgésie.
Analgésie
Lanalgésie postopératoire est fournie avec 0,1mg/kg de morphine par voie intramusculaire à quatre heures dintervalle sur demande et le temps de la première demande analgésique est noté. Chaque administration de morphine est précédée dune évaluation de la douleur du patient, de la tension artérielle, du rythme respiratoire et du degré de sédation (Echelle de sédation Ramsay Appendice II). De la morphine a été donnée seulement aux patients avec une échelle verbale simple > 1 (> légère douleur), avec une pression artérielle systolique de 100mmHg ou plus, avec un rythme respiratoire de plus de 8 et avec un score de sédation < 3 (Appendice II). Les patients qui ressentaient de la douleur malgré un dosage maximal de morphine ont reçu 10mg/kg de paracétamol (Drugamol)® par voie intraveineuse dans une infusion de saline normale sur une période de 15minutes en tant quanalgésie de secours. Les patients qui ont continué à se plaindre de douleur malgré les doses maximales danalgésiques et les patients qui ne voulaient plus continuer létude ont été autorisés à se retirer de létude et leur douleur a été activement contrôlée par le titrage des opioïdes. On a demandé à chaque patient dexprimer sa satisfaction de lanalgésie fournie.
Analyse de données
Les résultats générés de cette étude sont exprimés sous forme de fréquences ou de proportions de total, de moyennes et décarts-types. Les tests de signification sont aussi analysés avec le test t de Student pour les moyennes et le test chi carré pour les variables catégorielles en utilisant un progiciel informatique EPI-infoversion 2002. Une valeur p inférieure à 0,05 est considérée statistiquement significative.
RÉSULTATS
Un total de quarante-six (46) patients sont étudiés sur une période de six mois. Six patients sont exclus danalyses supplémentaires : 3 ont eu des médicaments non-stéroïdiens anti-inflammatoires prescrits par inadvertance par leurs médecins traitants en moins de six heures de la fin de lintervention chirurgicale, 2 se sont retirés volontairement et un avait lhypotension. Quarante patients ont complété létude. Vingt patients ont eu leurs plaies infiltrées avec 40mls de 0,25% de bupivacaïne pendant que les vingt autres ont eu leurs plaies infiltrées avec un volume égal de saline.
Lintervalle dâge des patients est entre 25 et 69 ans. Les patients dans le groupe témoin sont nettement jeunes que ceux dans le groupe détude (38,25 ±7,7 ans contre 44,75 ± 9,0 ans, p = 0,01).
Dans le groupe de témoin, 13 patients (65%) ont subit la myomectomie par rapport à 11 patients (55%) dans le groupe détude. Les autres ont subit une hystérectomie abdominale totale (tableau 1). Bien que plus de patients ont subit la myomectomie dans le groupe témoin que dans le groupe détude, la différence nest pas statistiquement significative (Valeur p du test bilatéral exact de Fishers = 0,7475).
Le temps moyen pour la demande analgésique dans le groupe témoin est nettement inférieur que dans le groupe détude (102 +/- 84,0min vs 174 ± 117,6 min, p<0,05). Six patients (30%) qui ont eu de la saline infiltrés dans la plaie ont demandé de lanalgésie en moins dune heure de la fin de la chirurgie alors que seulement un patient (5%) de ceux qui ont eu une infiltration de bupivacaïne dans la plaie a demandé de lanalgésie pendant la même période. Un patient dans le groupe détude (5%) a eu une période prolongée de soulagement de la douleur de 10 heures postopératoires. Bien que deux patients (10%) dans le groupe témoin ont eu une période étendue danalgésie postopératoire, cela na pas duré plus de cinq heures (Figure 1).
La dose moyenne de morphine reçue par la groupe témoin est de 33,5mg +/-3,94 (intervalle 20 40 mg) alors que celle du groupe détude est de 30,5mg +/-3,94 (intervalle 20 40mg). Même si les patients dans le groupe témoin ont reçu plus de morphine, la différence nest pas statistiquement significative (p = 0,0665).
Six (30%) patients dans le groupe témoin et 4 (20%) dans le groupe détude ont eu une analgésie de secours respectivement (Tableau 2). La différence nest pas statistiquement significative (Valeur p du test bilatéral exact de Fishers = 0,7164).
LIMPRESSION DES PATIENTS SUR LANALGÉSIE
Quand on a demandé aux patients leurs impressions de lanalgésie, 6 (30%) des patients dans le groupe témoin étaient légèrement satisfaits alors que 14 (70%) étaient modérément satisfaits (Tableau 3). Dans le groupe témoin, 3 (15%) étaient légèrement satisfaits, 16 (80%) étaient modérément satisfaits alors que 1 (5%) a rapporté quil était totalement satisfait. Les différences ne sont pas statistiquement significatives (Valeur p du test bilatéral exact de Fishers = 0.4506).
DISCUSSION
Les médicaments anesthésiques locaux deviennent de plus en plus à la mode pour la prise en charge des douleurs issues des interventions chirurgicales à cause de leurs propriétés analgésiques et labsence deffets indésirables provoqués par les opiacés. Cependant, malgré la popularité des stratégies anesthésiques locales pour lanalgésie somatique postopératoire, les données relatives à leur efficacité dans la réduction des besoins en opioïde sont contradictoires.
La dose totale de bupivacaïne utilisée pour chaque patient dans cette étude est 100mg. Ceci inclut les 20ml de 0,25% de bupivacaïne infiltrés dans les tissus sous-cutanés et les 20ml de 0,25% de bupivacaïne infiltrés dans lespace sous-aponévrotique. La concentration 0,25% est choisie parce quon la trouve efficace pour le blocage des nerfs sensoriels quand elle est utilisée pour lanalgésie postopératoire. 16 Une importante considération est le volume et la concentration de lanesthésie locale livrée au site de la chirurgie. Un large volume de solution (40ml de 0,25%) est choisi pour assurer une diffusion adéquate de la bupivacaïne aux fibres nerveuses.
Il y a différentes sources de douleur après une hystérectomie ou une myomectomie abdominale. Une contribution importante vient de la douleur des fibres viscérales qui sont responsables de la sensation de douleur profonde. Ces fibres ne sont pas accessibles au blocage par infiltration avec des agents anesthésiques locaux. Ceci pourrait expliquer le fait quil nétait pas possible de réaliser un soulagement total de la douleur (VRS = 0) avec aucun des patients.
La technique utilisée pour ladministration de lanesthésie locale est dune importance majeure. Une étude par Yndgaard et al montre que la lidocaïne est plus efficace quand appliquée de manière sous-aponévrotique par rapport à linfiltration sous-cutanée après la cure dune hernie.17 Tan et al trouvent aussi quune infiltration sélective du muscle grand dorsal entraîne la réduction des scores de douleurs et la consommation de morphine. 13 Ils concluent que le muscle droit est une source importante de douleur au début de la période postopératoire après lhystérectomie. Dans notre étude, les couches sous-cutanée et sous-aponévrotique de lincision chirurgicale sont infiltrées.
Le temps de la première demande analgésique est nettement retardé (p<0,05) dans le groupe détude par rapport au groupe témoin (Figure 1). Ceci est en accord avec létude dEgan et ses collègues qui trouvent que le temps de la première demande analgésique est nettement retardée chez les patients qui ont une infiltration aponévrotique avec la bupivacaïne après une laparotomie de confort que chez ceux qui ne lont pas. Dans leur étude, le temps de la première demande analgésique dans le groupe témoin est de 1,3 heures alors que celle du groupe détude est de 2,2 heures (p<0,05).18
En outre, une grande proportion de patients dans le groupe détude (75%) était sans douleur dans les deux premières heures après la chirurgie. Cette période est assez longue pour que lanalgésie postopératoire administrée à la fin de la chirurgie réalise une concentration plasmatique adéquate pour une transition en douceur de lanalgésie de la période intra-opératoire à celle postopératoire.
La douleur que beaucoup de patients ressentent dans lintervalle entre la fin de la chirurgie et lentrée en action des opiacés administrés dans la période postopératoire peut être efficacement soulagée par linfiltration de bupivacaïne dans la plaie. Cependant, la durée dans cette étude est très loin de la durée daction de 200 minutes de la bupivacaïne quand utilisée pour linfiltration, telle que documenté par Bukwirwa. 19 Cette apparente réduction dans la durée daction de la bupivacaïne est probablement due à leffet significatif de la douleur viscérale qui nest pas soulagée par linfiltration danesthésique locale dans la plaie. Bien que la période de lanalgésie peut être occasionnellement prolongée jusquà 10 heures comme cétait le cas avec un patient, leffet analgésique de linfiltration de bupivacaïne dans la plaie au-delà de deux heures ne peut être garanti. Cette durée de 10 heures a-t-elle été trouvée dans des études antérieures ? La dose moyenne de morphine administrée de manière postopératoire aux deux groupes sest révélée essentiellement similaire (Figure 2). Ce constat est similaire à celui de létude de Coby et Reid où linfiltration de la plaie pour certains des patients qui ont subit lhystérectomie na pas réduit les besoins en morphine. 20 Klein et al ont aussi trouvé quinfiltrer les couches superficielles et profondes de la plaie des patients post-hystérectomie ne réduit pas la consommation de la morphine.21 Bien que Tan et al ont révélé une réduction de la consommation de morphine chez les patients qui ont subit une hystérectomie, leur étude était limitée seulement aux six premières heures après lintervention chirurgicale.13 Zohar et ses collègues ont aussi révélé une réduction dans les besoins en opioïde suite à une infiltration avec la bupivacaïne mais lanesthésie locale a été livrée par lintermédiaire dun cathéter à travers un dispositif ACP aux patients qui ont subit une hystérectomie abdominale totale.22
Limpossibilité de découvrir une différence significative dans la consommation de morphine entre les deux groupes dans notre étude peut refléter un inconvénient dans la manière dont la morphine a été administrée dans létude. Quand lanalgésie morphinique intraveineuse est fournie par des systèmes danalgésie contrôlée par le patient (ACP), les patients consomment moins dopioïdes par rapport à ceux qui ont reçu une analgésie morphinique intramusculaire intermittente et ont un soulagement amélioré de la douleur. 23 En autorisant lauto-administration de lanalgésie, les systèmes ACP peuvent mettre en lumière des différences individuelles dans la consommation dantalgiques dues à divers degrés de sévérité de la douleur ressentie.
Bien quon ne sache pas les apports relatifs des diverses structures anatomiques à la douleur postopératoire dans cette étude, il est certain que si la douleur avait été principalement somatique, linfiltration de la plaie seule aurait probablement de manière adéquate soulagé la douleur. Limplication de ceci est que la composante viscérale de la douleur ne peut être ignorée dans ces procédures chirurgicales. Une autre explication possible est que la douleur provenant des viscères et des couches péritonéales plus profondes peut être une contributrice importante à la douleur globale ressentie que celle provenant des couches cutanées, sous-cutanées et musculaires dune blessure dans la détermination des besoins analgésiques. Les afférentes des structures plus profondes ne seraient pas touchées par linfiltration de la plaie. Cependant, quand on sest renseigné auprès des patients sur le site de leur douleur, seulement 30% des patients dans le groupe détude ont répondu quelle était profonde alors quun autre 30% a rapporté que la douleur était superficielle et 40% ont répondu quils éprouvaient de la douleur aux deux sites. Par contre, 55% des patients dans le groupe témoin ont rapporté quils éprouvaient de la douleur de manière superficielle. Bien quune faible proportion de patients dans le groupe détude ait rapporté une douleur superficielle, la différence nest pas statistiquement significative.
Une plus grande concentration ou un large volume de bupivacaïne pourrait être plus efficace pour maximiser leffet anti-nociceptif. Cependant, si cela est fait, une attention devrait être accordée aux signes de toxicité de bupivacaïne comme le frissonnement excessif, la nausée, le vertige, la confusion, les crises ou les arythmies cardiaques. La rapidité dabsorption de la bupivacaïne au plan aponévrotique pré-péritonéal avec augmentation subséquente de la concentration sanguine nest pas étudiée dans cette étude. Une enquête doit être menée dans ce sens avant dessayer daugmenter la dose pour cette procédure. Bien quune grande proportion de patients dans le groupe détude ont rapporté des dégrées supérieurs de satisfaction avec lanalgésie postopératoire, ce constat nest pas statistiquement significatif (Tableau 3). Ceci pourrait être le reflet de limportance relative de la douleur viscérale qui nest pas soulagée par une infiltration danesthésique locale dans la plaie.
Implications des constats : La routine qui consiste à infiltrer la bupivacaïne dans la plaie comme faisant partie du traitement analgésique postopératoire des patients sous hystérectomie ou myomectomie devrait être recommandé pour assurer une transition en douceur de lanalgésie intra-opératoire à celle postopératoire. Pour lefficacité de lanalgésie, il est important que les deux couches sous-aponévrotique et sous-cutané de la plaie soient infiltrées.
LIMITE DE LÉTUDE
Lanalgésie opioïde est fournie sous forme dinjections intramusculaires intermittentes. Il aurait été préférable dutiliser une technique analgésique contrôlée par le patient. Cependant, cela nétait pas possible parce que le matériel nétait pas disponible dans notre centre au moment de létude.
CONCLUSION
Linfiltration de bupivacaïne dans la plaie sert à augmenter les options disponibles pour le soulagement de la douleur postopératoire suite à une chirurgie abdominale basse de confort. Cependant, elle ne peut être utilisée comme seule agent analgésique. La technique a fourni une analgésie adéquate dans les deux premières heures après lintervention chirurgicale sans ladministration dopiacés.
Cela a aussi amélioré le score de douleur évalué par léchelle verbale simple dans les six premières heures au repos et dans les vingt-quatre premières heures postopératoires à la toux. Cependant, aucun effet dépargne morphinique na été constaté et la différence dans la demande danalgésie de secours nétait pas aussi statistiquement significative. Bien que les patients dans le groupe détude ne se soient pas trop plaints de la douleur superficielle et ont rapporté une meilleure satisfaction à lanalgésie, ces constats ne sont pas statistiquement significatifs.
REMERCIEMENTS
Nous remercions le personnel de la salle dopération et de la salle de gynécologie pour leur coopération. Les médecins résidents et les infirmières du département danesthésie ont joué un rôle inestimable dans le succès dans cette étude, nous leur sommes tous reconnaissants.
RÉFÉRENCES
- Kolawole IK, Fawole AA. Traitement de la douleur postopératoire suite à une césarienne au Centre Hospitalier Universitaire de lUniversité dIlorin, Nigeria. West Afr J Med 2003; 22: 305-309.
- Ocitti E.F et Adwork JA. La prise en charge de la douleur postopératoire suite dimportantes opérations abdominales et thoracique. East Afr Med J 2000; 77: 299-302
- Smith G. La douleur postopératoire. Dans Livre danesthésie. Aitkenhead AR et Smith G. (Editeur). 2ème édition. Longman Group UK Ltd 1990: 449-457.
- Faponle AF, Soyannwo OA Traitement de la douleur postopératoire : habitudes de prescriptions dans deux centres hospitaliers universitaires du Nigéria Niger J Med 2002 11 (4): 180-182
- McGuire L, Heffner K, Glaser R, Needleman B, Malarkey W, Dickinson S, Lemeshow S, Cook C, Muscarella P, Melvin WS, Ellison EC, Kiecolt-Glaser JK. La douleur et la cicatrisation de la plaie chez des patients chirurgicaux. Ann Behav Med. 2006 Apr;31(2):165-72.
- Sasseron AB, Figueiredo LC, Trova K, Cardoso AL, Lima NM, Olmos SC, Petrucci O. Est-ce que la douleur perturbe la fonction respiratoire après une chirurgie à cur ouvert ? Rev Bras Cir Cardiovasc 2009 Oct-Dec; 24(4):490-6
- Joshi GP, Ogunnaike BO. Conséquences du soulagement inadéquat de la douleur postopératoire et la persistance chronique de la douleur postopératoire Anesthesiol. Clin North America. 2005 Mar;23(1):21-36.
- Hanniball K, Galasius H. La bupivacaïne réduit les premiers et les derniers besoins en opioïdes après une hystérectomie. Anesth Analg 1996; 83:376-381.
- Johansson B. Glise H, Hallerback B, Dalman P, Kristoffersson A. Linfiltration locale préopératoire de ropivacaïne pour soulager la douleur postopératoire après cholécystectomie Anesth Analg1994; 78:210-214.
- Kushimo OT, Bode CO, Adedokun BO, Desalu I. Infiltration cicatricielle de bupivacaïne pour l'analgésie postopératoire chez les enfants. Afr J of Anaes Int care 2001; 4: 13-15.
- Tverskoy M, Cozacov C, Ayache M, Bradley EL, Kissin I. La douleur postopératoire après une herniorraphie inguinale avec différents types d'anesthésie Anesth Analg 1990; 70: 29-35.
- Jebeles JA, Reilly JS, Gutierrez JF, Bradley EL, Kissin I. L'effet de linfiltration pré-incisionnelle des amygdales avec la bupivacaïne sur la douleur suite à une amygdalectomie sous une anesthésie générale. Pain 1991; 47: 305-308.
- Tan CH, Kun KY, Onsiong MK, Chan MK, Chiu WKY, Tai CM. Linfiltration anesthésique locale post-incisionnelle du muscle droit diminue la première douleur et la consommation de morphine après hystérectomie abdominale. Acute Pain 2002;4: 49-52.
- Givens VA, Lipscomb GH, Meyer NL. Un essai randomisé de l'irrigation des plaies postopératoires avec un anesthésique local pour la douleur après une césarienne. Am J Obstet Gynecol 2002; 186: 1188-91.
- Cobby TF, Reid MF. Linfiltration de la plaie avec un anesthésique local après une hystérectomie abdominale. Brit J. Anaesth 1997; 78:431-2.
- Pettersson N, Berggren P, Larsson M, Westman B, Hahn RG. Soulagement de la douleur par infiltration de la plaie avec de la bupivacaïne ou de la ropivacaïne à haute dose après cure de hernie inguinale. Reg Anesth Pain Med. 1999 Nov-Dec;24(6):569-75.
- Yndgaard S, Holst P, Bjerre-Jepsen K, Thomsen CB, Struckmann J, Mogensen T. Lidocaïne administrée par voie sous-cutanée contre celle administrée par voie sous-aponévrotique dans le traitement de la douleur après une herniotomie inguinale. Anesth Analg. 1994;79:3247.
- Egan TM, Herman SJ, Doucette EJ, Normand SL, McLeod RS. Une étude randomisée et contrôlée afin de déterminer l'efficacité de l'infiltration aponévrotique de la bupivacaïne dans la prévention des complications respiratoires après chirurgie abdominale de confort. Surgery1988;104: 734-40.
- Bukwirwa HW. La toxicité des médicaments anesthésiques locaux. Mise à jour en anesthésie. 1999; 10: 50-51.
- Cobby TF, Reid MF. Linfiltration de la plaie avec un anesthésique local après une hystérectomie abdominale. Brit J Anaesth1997; 78:431-2.
- Klein JR, Heaton JP, Thompson JP, Cotton BR, Davidson AC, Smith G. L'infiltration de la paroi abdominale avec un anesthésique local après une hystérectomie abdominale totale n'a pas d'effet d'épargne morphinique. Brit J Anaesth 2000; 84:248-249.
- Zohar E, Fredman B, Phillipov A, Jedeikin R, Shapiro A. L'efficacité analgésique de l'instillation de la bupivacaïne dans la blessure après une hystérectomie abdominale totale avec salpingo-ovariectomie bilatéral. Anesth Analg 2000;91 :1436-1440.
- Morgan GE, Mikhail MS, Murray MJ. Traitement de la douleur. Dans : Anesthésiologie clinique. 4ème édition. New York: Lange Medical Books/McGraw-Hill Medical Publishing Division, 2006. 359-411
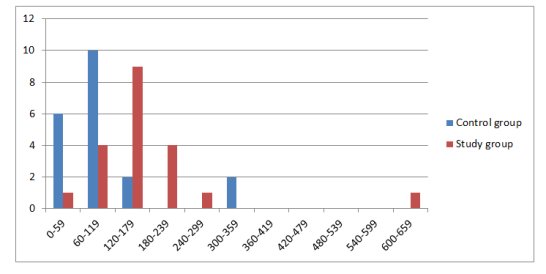
FIGURE 1: HEURE DE LA PREMIÈRE DEMANDE ANALGÉSIQUE
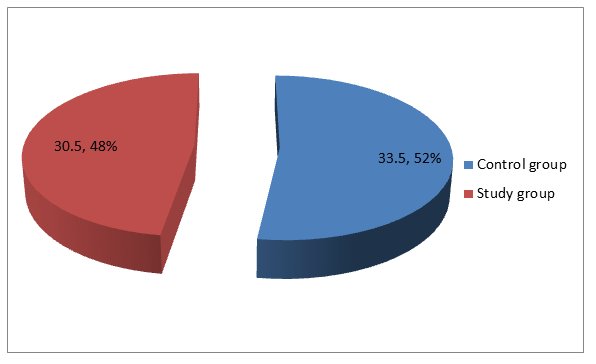
FIGURE 2: MOYENNE DE CONSOMMATION DE MORPHINE
| TABLE 1: TYPE DINTERVENTION CHIRURGICALE |
|
|
CONTROL GROUP |
STUDY GROUP |
TOTAL |
|
MYOMECTOMY |
13 (65%) |
11 (55%) |
24 |
|
TOTAL ABDOMINAL HYSTERECTOMY |
7 (35%) |
9 (45%) |
16 |
|
TOTAL |
20 |
20 |
40 |
| TABLE 2: DEMANDE DANALGÉSIE DE SECOURS |
|
|
CONTROL GROUP |
STUDY GROUP |
TOTAL |
|
YES |
6 |
4 |
10
|
|
NO
|
14 |
16 |
30
|
|
TOTAL |
20 |
20 |
40
|
| TABLE 3: LIMPRESSION DES PATIENTS SUR LANALGÉSIE |
|
|
CONTROL GROUP |
STUDY GROUP |
TOTAL |
|
DISSATISFIED |
0 |
0 |
0 |
|
MILDLY SATISFIED |
6 (30%) |
3 (15%) |
9 |
|
MODERATELY SATISFIED |
14 (70%) |
16 (80%) |
30 |
|
FULLY SATISFIED |
0 |
1 (%) |
1 |
|
TOTAL |
20 |
20 |
40 |
APPENDICE I
Echelle verbale simple
Cest un instrument de mesure utilisé pour évaluer le niveau de la douleur. Cest simple, subjectif et applicable même aux patients illettrés parce que cest facile à comprendre. On la traduit en langue yorouba, ce qui le rend particulièrement utilisable parmi la population visée. Echelle verbale simple.
| Verbal rating scale | ||
| Français | Yoruba | |
| 0. | Pas de douleur | Ko si irora |
| 1. | Douleur légère | Irora die |
| 2. | Douleur modérée | Irora pupo |
| 3. | Douleur sévère | Irora to ga |
| 4. | Douleur atroce | Irora to koja afarada |
APPENDICE II
Echelle de sédation Ramsay
- Anxieux et agité
- Coopérant, orienté et tranquille
- Répond aux commandes verbales seulement
- Endormi mais réponse rapide à un stimulus auditif fort / à un petit coup glabellaire
- Endormi mais réponse lent à un stimulus auditif fort / à un petit coup glabellaire
- Endormi, pas de réponse